Sono note molte metodiche per preparare queste polveri, la più diffusa come si può vedere dalle numerose pubblicazioni scientifiche disponibili sul web, utilizza idrazina idrato come riducente.
Questa mia sintesi è innovativa e prevede l’azione del solfato di idrazina su una soluzione acquosa di un sale di Nichel in ambiente basico.
In soluzione acquosa ho sfruttato la seguente reazione:
2N
2H
4.H
2SO
4 + 4NaOH ---> 2N
2H
4 + 2Na
2SO
4 + 4H
2O
Naturalmente l’idrazina me la ritrovo in soluzione in forma idrata 2N
2H
4.H
2O, di seguito il procedimento usato.
Materiale ed attrezzatura usata: beuta da 250cc, piastra riscaldante, agitatore ad asta
(F. 1A); imbuto filtrante con carta da filtro e pompa da vuoto
(F.1B)

Reagenti :
-
A) soluzione di 10 gr. di NiSO
4-7H
20 in 100 ml H
2O
-
B) soluzione di NaOH al 20% (100ml)
-
C) solfato di idrazina
Procedura :
Portare la soluzione
A a 70ºC
(F 2A) e sotto agitazione continua aggiungere 12 gr di idrazina solfato, molto lentamente a piccole porzioni finche si è sciolta quasi del tutto (tempo impiegato per questa operazione 20 min.) a questo punto la soluzione si presenta torbida con precipitato in sospensione come sotto
(F2 B)

a questo punto sempre sotto agitazione ed a 70ºC, aggiungere lentamente con pipetta parte della soluzione
B sino a portare la soluzione
A a pH 8 – 8,5, (è sufficiente il controllo con cartina indicatrice) la soluzione diventa blu con abbondante precipitato, segno della formazione di un complesso Ni-idrazina
(F2 C), (tempo impiegato 15 min, quantità di sol.
B usata circa 22ml) per il completamento della reazione lasciare tutto fermo sotto agitazione per 20 min.
Iniziare una nuova aggiunta sempre lentamente di sol
B sino a portare il pH a 12,5 – 13,00 controllare il valore con cartina all’indicatore (tempo impiegato in questa fase 15 min sol.
B usata 36 ml) dopo un po’ la soluzione diventa per un breve istante rosa e poi subito dopo viola
(F2 D)
Lasciare che la reazione proceda da sola se il pH si abbassa correggerlo con sol NaOH dopo 20 min circa la soluzione vira prima verso un verde sporco
(F2 E) poi verso un grigio
(F2 F), la reazione diventa esotermica e la temperatura potrà salire sino a 80ºC e si noterà una lieve ebollizione del preparato.
Per completarsi la reazione richiede ulteriori 1 od anche 2 ore con temp. da 70 a 80 ºC. e sarà completa quando non vi sarà più ebollizione, fermato l’ agitatore il precipitato sarà grigio-nero con supernatante biancastro lattiginoso
(F2 G).
Il sedimento va estratto e sottoposto a ripetuti lavaggi con H
2O distillata preferibilmente a 40ºC seguiti da decantazione ed eliminazione del supernatante sino a pH neutro e sino a che il supernatante diventa trasparente. Filtrare il precipitato su imbuto con carta da filtro (F1 B), e mettere il prodotto in campana sotto vuoto per la completa essicazione.
Quello che si ottiene è una polvere di Ni da circa 100 nm . (valutata con osservazione al microscopio ottico,
confrontandola con polveri analoghe) a questo riguardo da tenere presente il limite minimo di risoluzione di un microscopio ottico che usando un obbiettivo ad immersione è di circa 200 nm. Quindi i 100 nm non sono visibili, mentre è valutabile una polvere nota da 1000 nm che mi serve da riferimento Nella
(F 3) un confronto con polvere di Ni da 50–100 µm.

La polvere ottenuta contiene Ni(OH)
2 e NiO, per ottenerla pura priva di ossidi ed idrati va trattata ad alta temperatura 200 – 400 ºC prima sotto vuoto e poi con idrogeno, e questa è la fase successiva della preparazione.
Purificazione di polveri di nichel da idrati ed ossidi.
Il trattamento viene eseguito prima sotto vuoto e poi in atmosfera di idrogeno a 310ºC.
La prima fase prevede l’eliminazione di Ni(OH)
2 che si decompone a 220-230ºC:
a temp. > 220ºC Ni(OH)
2 --> NiO + H
2O.
Quindi riduzione dell’ossido in atmosfera idrogeno:
NiO + H
2 --> Ni + H
2O.
Attrezzatura usata: fornetto ad induzione, bombola da 0,5l con H
2 a 10 bar
(F4) e pompa da vuoto a doppio stadio.
Reagenti: polvere di Ni 100nm da precedente reazione
(F3), H
2.

La procedura è sinteticamente raffigurata nel grafico di
(F 5)
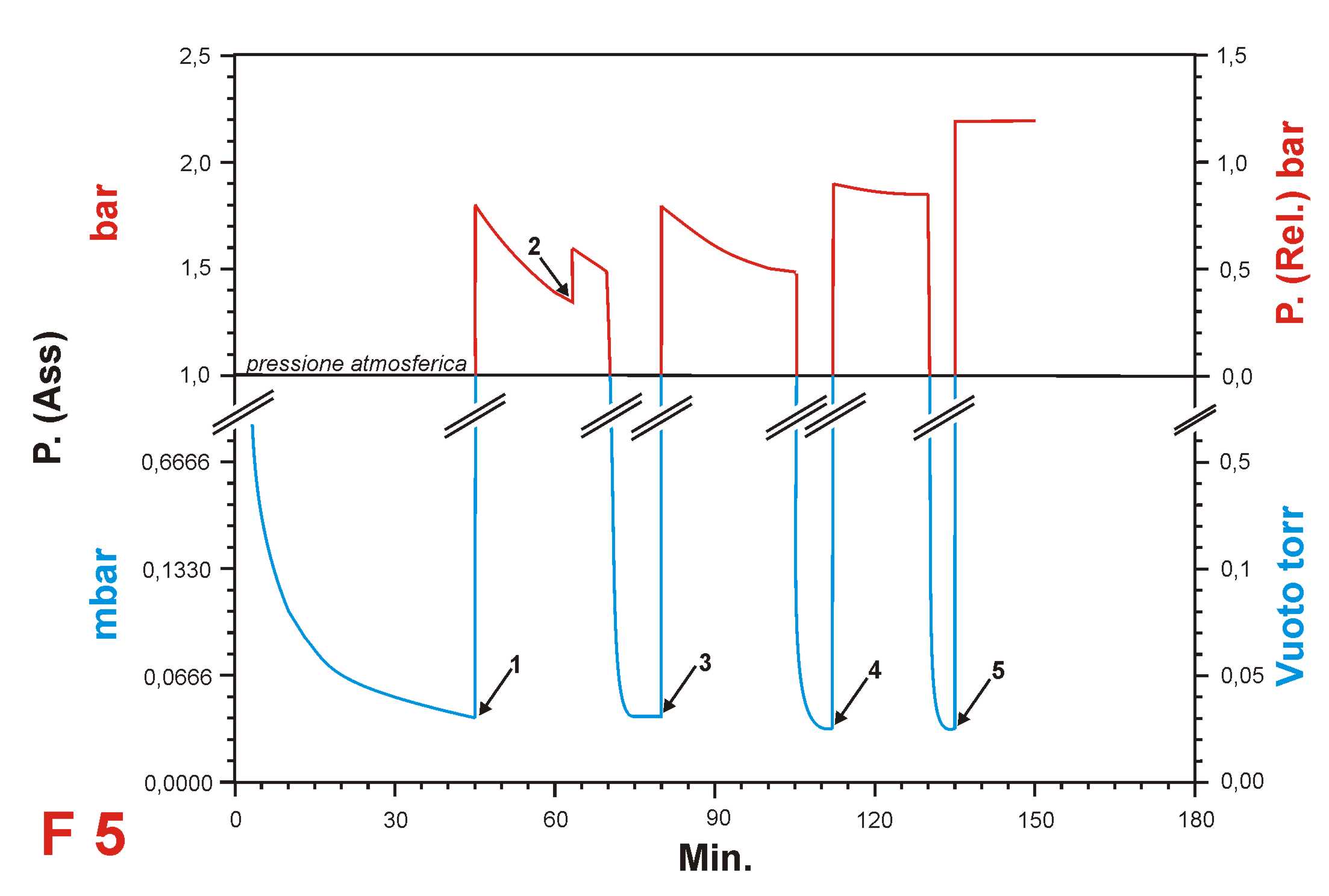
Nelle ordinate, a sinistra è riportata la pressione assoluta (bar e mbar) all’interno del crogiolo, a destra quella relativa (in bar ed in torr per quanto riguarda il vuoto), in ascisse i tempi (minuti).
Caricati nel crogiolo 1 gr di polvere di Ni , attaccata la pompa da vuoto e contemporaneamente acceso il forno che dopo 10 min raggiunge i 310 ºC impostati.
Dopo 45 min il vuoto è di 0,03 torr e l’ idrato di nichel presente nelle polveri si è tutto decomposto in NiO ed H
20 allo stato di vapore, subito eliminato dalla pompa da vuoto.
Al punto 1 del grafico chiuso il rubinetto d’aspirazione viene immesso H
2 sino a 0,8 bar si nota che in 20 min la pressione dell’ H
2 scende a 0,35 bar, inequivocabile segno che indica l’inizio della riduzione dell’ossido di nichel, al punto 2 la pressione di H
2 e stata riportata a 0,6 bar a questo punto si notano gocce d’ H20 di condensa all’interno della finestrella d’osservazione del crogiolo
(F 6)

La finestrella superiore del crogiolo è mantenuta a temp. di 70-80 ºC da una continua ventilazione.
Dopo 70 min. il crogiolo viene svuotato del suo contenuto allo stato di gas (H
2 e vapore d’H
20) ed il vuoto
è riportato a 0,03 torr. Al punto
3 vien rifatta la carica di H
2, l’operazione viene ripetuta ai punti
4 e
5 sino a che, dopo la ricarica del punto
5 a 1,2 bar si nota che la pressione dopo 15 min. resta costante la reazione è finita, Spento il fornetto e lasciato raffreddare il tutto viene liberato l’ idrogeno e si recupera la polvere metallica.
Risultati: da 1 gr di polvere introdotti nel fornetto ora mi ritrovo 0,9 gr di polvere metallica, 0,1 gr erano costituiti da gruppi OH e da O
2.
Da una prima osservazione tra la polvere prima del riduzione
(F 7A) e dopo l’eliminazione di ossidi ed idrati
(F 7B) si nota subito che la polvere è passata dal grigio scuro al nero.
Questa polvere metallica è molto reattiva e volatile, per proteggerla dall’ossidazione va conservata sotto gas inerte in genere argon.

Bibliografia:
-
preparation of ultrafine nickel powder
-
Method for preparing nickelfine powder
-
Synthesis of Nano-sized Nickel Particles by a Bottom-up Approach in the Presence of an Anionic Surfactant and a Nonionic Polymer






